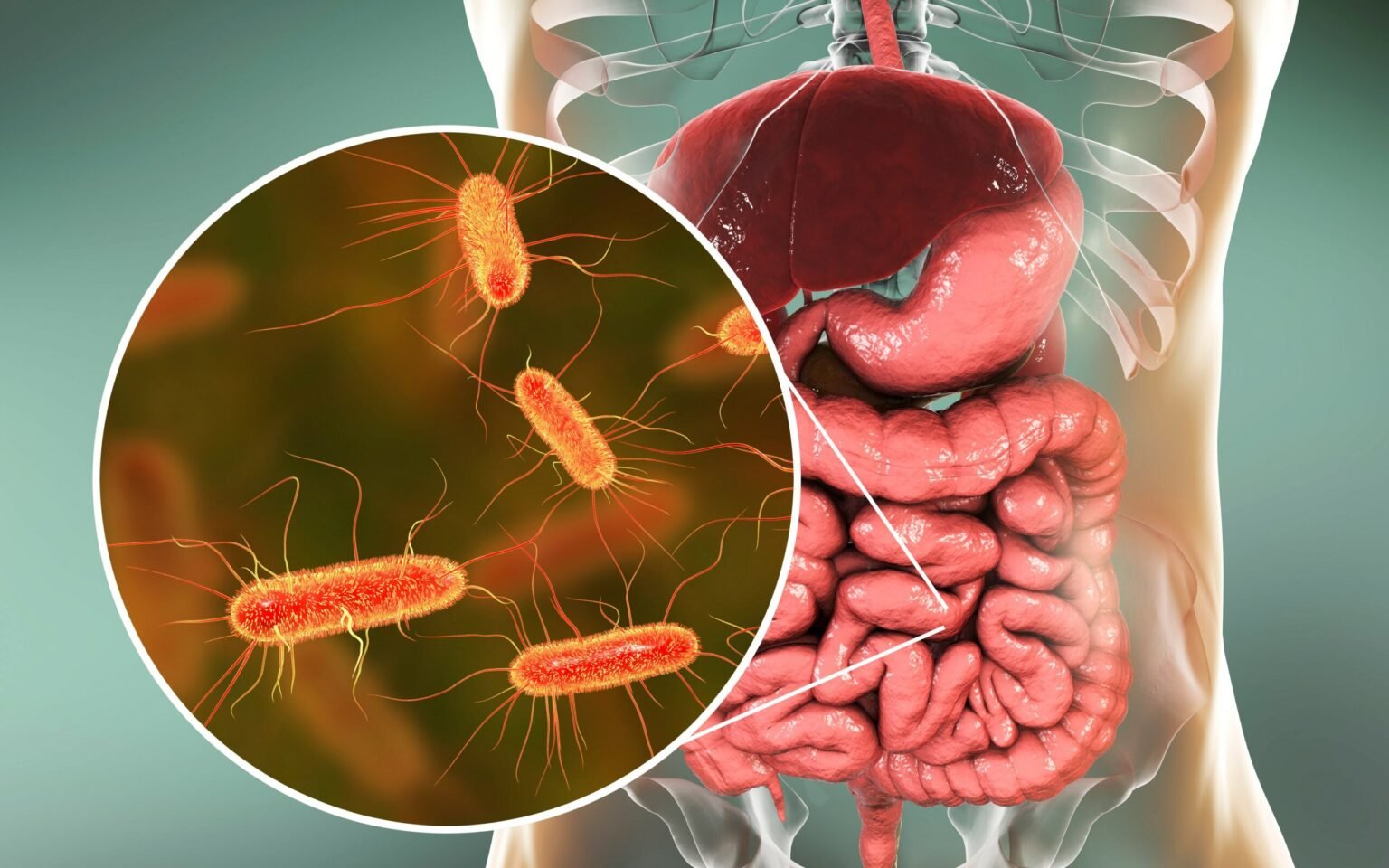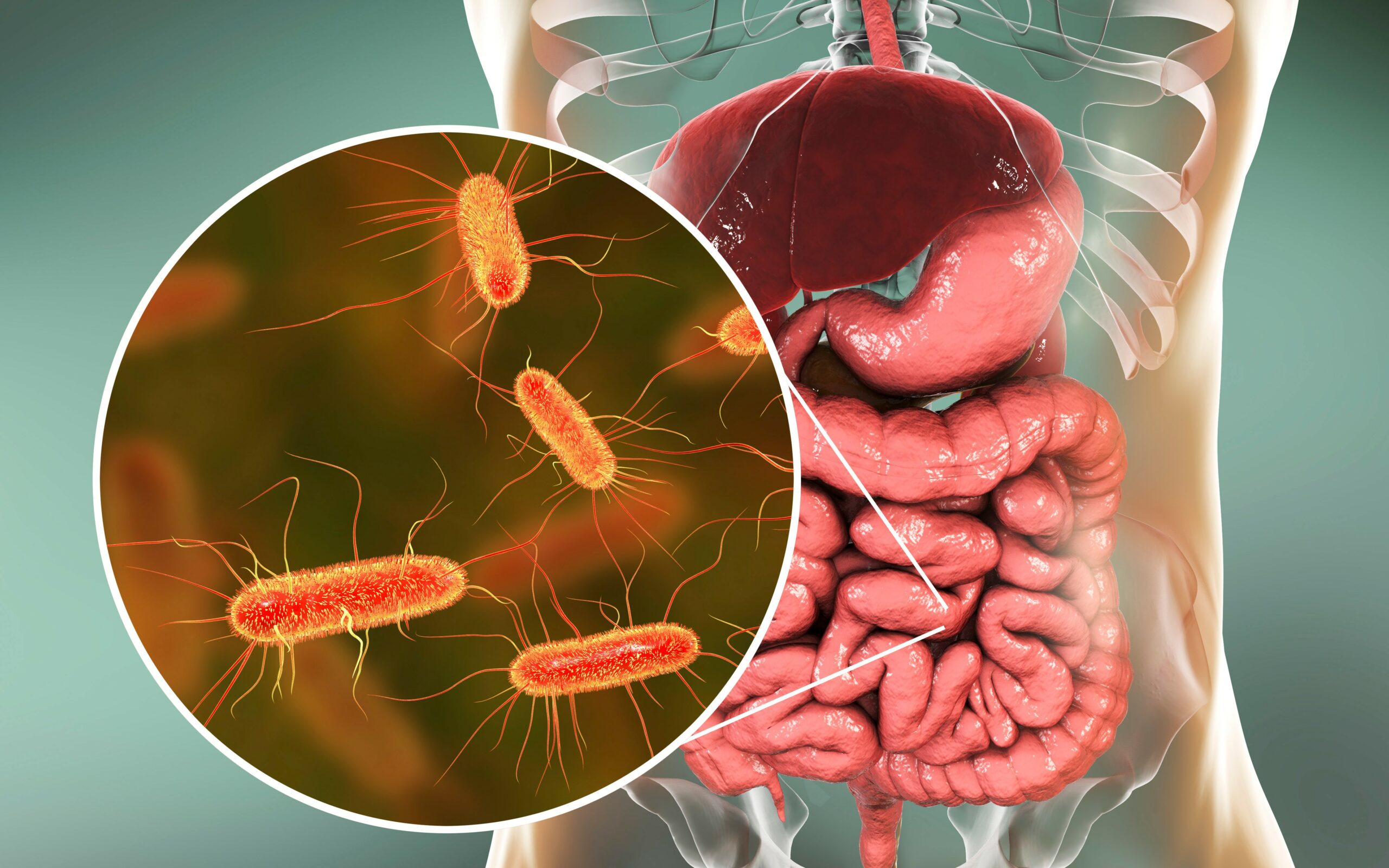
Estudos recentes indicam que a composição da microbiota intestinal desempenha um papel crucial na determinação da eficácia dos tratamentos de imunoterapia para o câncer. Essa descoberta, que surge com a ascensão da imunoterapia como uma revolução no combate à doença, posiciona o intestino como um órgão de relevância fundamental na resposta do organismo às terapias oncológicas.
O intestino humano abriga trilhões de microrganismos, incluindo vírus, fungos e bactérias, que formam a complexa microbiota intestinal. Considerada por muitos como um órgão extra, essa comunidade microbiana é essencial para processos como a digestão e a produção de vitaminas, mas, mais significativamente, atua no treinamento do sistema imunológico. A imunoterapia, diferentemente da quimioterapia que ataca células de rápida multiplicação, age removendo os ‘freios’ que impedem o sistema imunológico de reconhecer e combater as células tumorais.
A relevância da microbiota é sublinhada pelo fato de que entre 70% e 80% das células do sistema imunológico estão localizadas na parede intestinal, em constante interação com esses microrganismos. Pesquisas recentes identificaram que a presença de certas bactérias está associada a um microambiente tumoral mais propício à ativação imune. Por outro lado, estados de disbiose, caracterizados por um desequilíbrio na flora intestinal e frequentemente ligados a inflamações crônicas, podem contribuir para a resistência ao tratamento imunoterápico. Perfis específicos da microbiota, conhecidos como Gut OncoMicrobiome Signatures (GOMS), emergem como potenciais biomarcadores para prever a resposta dos pacientes à imunoterapia.
O uso de antibióticos, por exemplo, merece atenção especial, pois uma meta-análise abrangente com mais de 46 mil pacientes demonstrou que sua administração pouco antes ou no início da imunoterapia está ligada a piores desfechos clínicos. Isso ocorre porque, ao eliminar bactérias patogênicas, os antibióticos também reduzem microrganismos benéficos, alterando o equilíbrio intestinal e comprometendo a resposta imune. Outra área de interesse é o transplante de microbiota fecal, já bem-sucedido no tratamento de infecções graves por *Clostridium difficile*. Estudos com pacientes de melanoma avançado que não respondiam à imunoterapia mostraram que a transferência de microbiota de respondedores levou parte deles a reagir ao tratamento, sugerindo uma ‘reprogramação’ do sistema imunológico.
A microbiota intestinal é notavelmente modulável, e a alimentação desempenha um papel central nesse processo. Dietas ricas em fibras, com consumo regular de frutas, verduras, legumes, grãos integrais e sementes, promovem o crescimento de bactérias benéficas, enquanto a variedade alimentar é crucial para a diversidade microbiana. Por outro lado, o uso indiscriminado de antibióticos, o consumo frequente de alimentos ultraprocessados e o uso inadequado de probióticos, inibidores de bomba de prótons e laxativos podem comprometer esse ecossistema.
O futuro do tratamento do câncer se desenha cada vez mais integrado e sistêmico, considerando não apenas o tipo do tumor, mas todo o ecossistema do organismo do paciente. É provável que, em breve, exames de fezes para análise da microbiota se tornem rotina antes da imunoterapia, permitindo que médicos prescrevam dietas de precisão ou ‘coquetéis de bactérias’ específicos para otimizar a resposta ao tratamento.